Buněčné stárnutí a stárnutí - Co můžete udělat
Mnoho lidí je poněkud obeznámeno se slovem „senescence“ a považují tento termín za synonymum stárnutí. Koneckonců, kořen slova je „sen-“, což znamená starý, a je také kořenem slova „senilní“, které samozřejmě znamená charakteristický pro stáří.
Když však biologové hovoří o buněčné senescenci, nemají přesně na mysli stárnutí tak, jak si lidé obvykle tento proces představují. V závislosti na typu tkáně žijí buňky ve vašem těle různě dlouhou dobu. Bílé krvinky mají životnost přibližně 13 dní, ve srovnání se 120 dny, které žije červená krvinka. Tukové buňky žijí přibližně osm let a střevní buňky (s výjimkou výstelky) žijí téměř 16 let.
Když buňky těla dosáhnou konce svého přirozeného života, umírají naprogramovanou smrtí prostřednictvím procesu zvaného apoptóza (řekněte „a-pop-TOE-sis“), který je navržen tak, aby nepoškodil žádné okolní buňky. Nebo možná je buňka mladá nebo ve středním věku a je nějakým způsobem poškozena. Mnohokrát lze toto poškození opravit a buňka obnoví svou normální funkci. Pokud je poškození příliš závažné, buňka opět podstoupí apoptózu a je zničena.
Normálně buňky neustále procházejí dělením, aby nahradily buňky, které odumřely, a také aby pomohly při opravě, například růstem nových kožních buněk k uzavření rány. Někdy, když je poškozena buněčná DNA, tyto buňky se stanou rakovinnými a začnou se nekontrolovaně množit.
Pochopení buněčného stárnutí
Jiný způsob, jakým buňky reagují na poškození, které není tak závažné, aby spustilo apoptózu, je stát se senescentními. To znamená, že místo toho, aby se nekontrolovaně množily, jednoduše přestanou dělit a normální buněčný cyklus končí. Mnoho vědců věří, že tato schopnost přejít do senescentního stavu je způsobem, jakým se tělo snaží zabránit tomu, aby se tyto poškozené buňky staly rakovinnými.
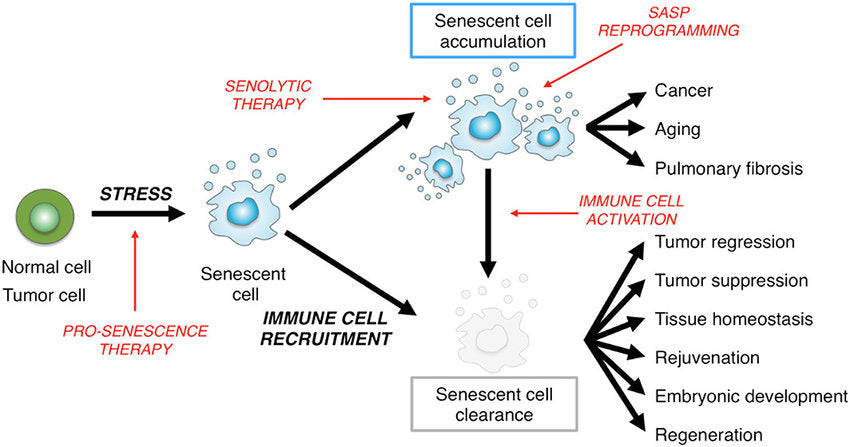
Ačkoli tyto senescentní buňky aktivně nedělí, rozhodně nejsou mrtvé. Senescentní buňky jsou stále velmi metabolicky aktivní, vylučují řadu proteinů a dalších molekul označovaných jako SASP (senescence-associated secretory phenotype), které mohou způsobovat zánět. Tímto způsobem mohou senescentní buňky signalizovat imunitním buňkám, aby přišly pomoci s odstraněním poškození a s opravou tkání. Zatím to vypadá jako dobrá věc.
I když SASP pomáhá při opravě tkání, některé proteiny a molekuly, které mohou tvořit tuto sadu, mohou mít škodlivé účinky. Jak stárnete, senescentní buňky se začínají hromadit v těle, včetně mozku. Tyto senescentní buňky všechny produkují zánětlivé molekuly a proteiny SASP, které mohou ve skutečnosti urychlit samotné stárnutí a zhoršit věkem podmíněné stavy, jako jsou srdeční choroby a Alzheimerova choroba. Navíc dlouhodobé vystavení SASP může ve skutečnosti vyvolat senescenci u jinak zdravých buněk.
Odstraňování senescentních buněk z těla
Co kdyby tyto senescentní buňky mohly být odstraněny z těla spolu s toxickými zánětlivými SASP proteiny a molekulami, které produkují? Již bylo prokázáno, že v myším modelu neurodegenerativního onemocnění zlepšuje odstranění senescentních buněk funkci mozku u těchto zvířat.
Ale co nebylo známo, je toto: mohlo by odstranění senescentních buněk z těla pomoci zmírnit stárnutí mozku a kognitivní úpadek, který přichází s normálním stárnutím? Nedávný výzkum vedený vědci z Robert and Arlene Kogod Center on Aging na Mayo Clinic, publikovaný v čísle časopisu Aging Cell ze dne 21. ledna 2021, se pokusil odpovědět na tuto otázku.
Výzkumníci se opět obrátili na myší model ve snaze odpovědět na tuto otázku. Tým použil transgenní myši. Tyto myši jsou speciálně vyšlechtěny pro lékařský výzkum a mají do jádra oplodněného myšího vajíčka vloženou „cizí“ DNA. Když se myš vyvíjí, cizí DNA se stává součástí každé buňky. Tyto speciálně vyšlechtěné myši umožnily týmu použít lék, který selektivně zabíjí buňky exprimující P16ink4a, protein zapojený do regulace buněčného cyklu a který zpomalí dělení buněk.
Jak organismy stárnou, zvyšuje se exprese proteinu P16ink4a. To pomáhá tělu snížit proliferaci kmenových buněk, což snižuje riziko rakoviny, ale zároveň činí tělo náchylným k účinkům proteinů SASP a dalších molekul, které tyto senescentní buňky produkují. Protože tento přístup nemohl zaručit zničení všech senescentních buněk, výzkumníci také použili kombinovaný koktejl léků k cílení na zbývající senescentní buňky u myší. Výzkumníci použili několik kohort starých myší (25 až 29 měsíců) a také mladší skupinu jako srovnání.
Výsledky byly zcela jasné: odstranění senescentních buněk v tělech a mozcích starých myší vedlo ke zmírnění věkem podmíněného kognitivního poškození, konkrétně dysfunkce prostorové paměti. Výsledky také ukázaly snížení markerů senescence v neuronech hipokampu, části mozku specificky spojené s pamětí a kognicí, která je vystavena progresivnímu zhoršování s věkem.
Odstranění senescentních buněk také významně snížilo markery zánětu mozku, který je jasně spojen s věkem podmíněným kognitivním postižením. Autoři zdůrazňují, že stále není zcela jasné, jak přesně buněčná senescence ovlivňuje stárnutí mozku, ale výsledky jejich studie jednoznačně ukazují, že terapie zaměřené na odstranění senescentních buněk poskytují slibný přístup k omlazení stárnoucího mozku a ke zlepšení paměti u starších lidí.
NAD a buněčné stárnutí
Jak jsme uvedli v předchozích článcích, NAD (nikotinamid adenin dinukleotid), který v těle působí jako důležitý koenzym nebo kofaktor a přirozeně klesá s věkem, vykazuje velmi slibné výsledky v oblasti proti stárnutí, včetně oblasti buněčné senescence. Výzkum z University of Queensland v Austrálii, publikovaný v čísle Cell Reports ze dne 18. února 2020, ukázal, že relativně nízké dávky NMN byly účinné při obnově kvality vajíček u starších myší. Ačkoli byl počáteční výzkum proveden na myších, vědci jsou velmi optimističtí ohledně příslibu těchto látek při léčbě lidské plodnosti.
Výzkumníci jednoznačně prokázali na myších modelech, že léčba NAD poskytuje silné anti-agingové účinky na neurovaskulární systém, včetně zlepšení kognitivního výkonu. Dále léčba vaskulárních buněk ze stárnoucích krys (biologický věk 24měsíčních myší odpovídá přibližně 60letým lidem), které byly po dobu pěti dnů ošetřeny NMN, ukázala obnovení mladistvých hladin NAD a návrat mitochondriální funkce. Také jsme jinde diskutovali, že NAD hraje klíčovou roli v optimálním fungování sirtuinů (říká se „sir-TWO-ins“), rodiny proteinů známých jako geny dlouhověkosti, které regulují buněčné stárnutí.
I když bylo prokázáno, že praktiky jako kalorická restrikce a půst zvyšují hladiny NAD, každodenní užívání vysoce kvalitního doplňku NAD+ je nejspolehlivějším, nejpraktičtějším a nejúčinnějším způsobem, jak si být jistý, že splňujete své potřeby NAD.
Kompletní informace o všech našich kvalitních NAD+ doplňcích naleznete zde, včetně NAD+ a jeho prekurzoru NMN. Denní užívání NAD+ doplňků zvýší vaše hladiny tohoto silného koenzymu a poskytne vám tu nejlepší ochranu proti účinkům stárnutí, včetně škodlivých účinků stárnutí na vaše kognitivní zdraví.
Reference:
1. Ogrodnik, M., Evans, S.A., Fielder, E., Victorelli, S., Kruger, P., Salmonowicz, H., Weigand, B.M., Patel, A.D., Pirtskhalava, T., Inman, C.L., Johnson, K.O., Dickinson, S.L., Rocha, A., Schafer, M.J., Zhu, Y., Allison, D.B., von Zglinicki, T., LeBrasseur, N.K., Tchkonia, T., Neretti, N., Passos, J.F., Kirkland, J.L. a Jurk, D. (2021), Odstranění senescentních buněk z celého těla zmírňuje věkem podmíněný zánět mozku a kognitivní poruchy u myší. Aging Cell, 20: e13296. https://doi.org/10.1111/acel.13296.
2. Bertoldo et al. Obnovení NAD zachraňuje ženskou plodnost během reprodukčního stárnutí. Cell Reports, 2020; 30 (6): 1670 DOI: 10.1016/j.celrep.2020.01.058
Kiss T & Nyúl-Tóth Á et al. Suplementace nikotinamid mononukleotidu (NMN) podporuje neurovaskulární omlazení u starých myší: transkripční stopa aktivace SIRT1, ochrana mitochondrií, protizánětlivé a anti-apoptotické účinky. Geroscience. 2020 duben;42(2):527-546. doi: 10.1007/s11357-020-00165-5. Epub 2020 únor 13. PMID: 32056076; PMCID: PMC7206476.
3. Tarantini S & Valcarcel-Ares MN et al. Suplementace nikotinamid mononukleotidem (NMN) obnovuje funkci cerebromikrovaskulárního endotelu a odpovědi neurovaskulární vazby a zlepšuje kognitivní funkce u starých myší. Redox Biol. 2019 červen;24:101192. doi: 10.1016/j.redox.2019.101192. Epub 2019 duben 10. PMID: 31015147; PMCID: PMC6477631.
4. Hou Y, Lautrup S, Cordonnier S, et al. Přidání NAD+ normalizuje rysy Alzheimerovy choroby. Proceedings of the National Academy of Sciences únor 2018, 115 (8) E1876-E1885; DOI:10.1073/pnas.1718819115.
5. Kiss T, Giles C, Tarantini S. et al. Suplementace nikotinamid mononukleotidem (NMN) podporuje anti-aging profil exprese miRNA v aortě starých myší, což předpovídá epigenetické omlazení a anti-aterogenní účinky. FASEB Journal 18. dubna 2020 https://doi.org/10.1096/fasebj.2020.34.s1.04769.


