Cellulær Senescens og Aldring - Hvad Du Kan Gøre
Mange mennesker er nogenlunde bekendt med ordet "senescence" og ligestiller begrebet med at være synonymt med aldring. Når alt kommer til alt, er roden af ordet "sen-", der betyder gammel, og det er også roden af ordet "senil", som selvfølgelig betyder karakteristisk for alderdom.
Men når biologer taler om cellulær senescens, mener de ikke præcis aldring på den måde, folk normalt tænker på denne proces. Afhængigt af typen af væv lever celler i din krop i varierende længder af tid. Hvide blodlegemer har en levetid på omkring 13 dage, sammenlignet med de 120 dage, en rød blodcelle lever. Fedtceller lever omkring otte år, og tarmceller (eksklusive slimhinden) lever næsten 16 år.
Når kroppens celler når slutningen af deres naturlige liv, dør de en programmeret død via en proces kaldet apoptose (udtales "a-pop-TOE-sis"), som er designet til ikke at skade nogen nærliggende celler. Eller måske er en celle ung eller midt i livet og er beskadiget på en eller anden måde. Mange gange kan denne skade repareres, og cellen genoptager sin normale funktion. Hvis skaden er for alvorlig, gennemgår cellen igen apoptose og bliver ødelagt.
Normalt gennemgår celler konstant deling, både for at erstatte celler, der er døde, og også for at hjælpe med reparation, som når nye hudceller vokser for at lukke et sår. Nogle gange, når cellulært DNA er beskadiget, bliver disse celler kræftfremkaldende og kastes ud i ukontrolleret proliferation.
Forståelse af cellulær senescens
Den anden måde, celler reagerer på skader, der ikke er så alvorlige, at de udløser apoptose, er ved at blive senescente. Dette betyder, at i stedet for at spirale ind i ukontrolleret proliferation, stopper de simpelthen med at dele sig, og den normale cellecyklus afsluttes. Mange forskere mener, at denne evne til at gå ind i en senescent tilstand er kroppens måde at forsøge at forhindre, at disse beskadigede celler bliver kræftfremkaldende.
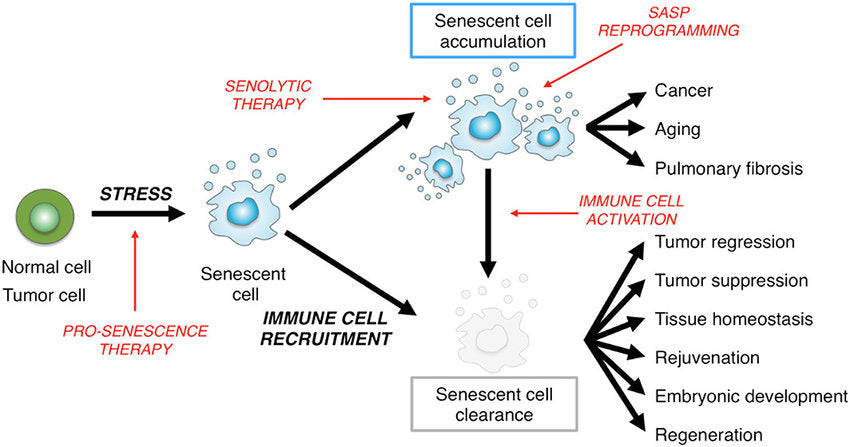
Selvom disse senescente celler ikke aktivt deler sig, er de på ingen måde døde. De senescente celler er stadig meget metabolisk aktive og udskiller en række proteiner og andre molekyler, der kaldes SASP (senescence-associated secretory phenotype), som kan forårsage inflammation. På denne måde kan de senescente celler signalere til immunceller om at komme ind for at hjælpe med at rydde op i skader og hjælpe med vævsreparation. Indtil videre ser dette ud til at være en god ting.
Men selvom SASP hjælper med vævsreparation, kan nogle af de proteiner og molekyler, der udgør dette spektrum, have skadelige virkninger. Når du bliver ældre, begynder senescente celler at ophobe sig i kroppen, inklusive hjernen. Disse senescente celler producerer alle SASP-inflammatoriske molekyler og proteiner, som faktisk kan fremskynde aldring i sig selv og forværre aldersrelaterede tilstande som hjertesygdomme og Alzheimers. Desuden kan vedvarende eksponering for SASP faktisk inducere senescens i ellers sunde celler."}
Fjernelse af senescente celler fra kroppen
Hvad hvis disse senescente celler kunne fjernes fra kroppen sammen med de giftige inflammatoriske SASP-proteiner og -molekyler, de producerer? Det er allerede blevet vist, at i en musemodel af neurodegenerativ sygdom har fjernelsen af senescente celler vist sig at forbedre hjernefunktionen hos disse dyr.
Men hvad der ikke var kendt, er dette: kunne fjernelsen af senescente celler fra kroppen hjælpe med at lindre hjerneældning og kognitiv tilbagegang, der følger med normal aldring? Ny forskning ledet af forskere ved Mayo Clinic's Robert and Arlene Kogod Center on Aging, offentliggjort i udgaven af tidsskriftet Aging Cell den 21. januar 2021, forsøgte at besvare dette spørgsmål.
Forskerne vendte igen tilbage til en musemodel i deres forsøg på at besvare dette spørgsmål. Holdet brugte transgene mus. Disse mus er specifikt avlet til at være en del af medicinsk forskning og har "fremmed" DNA indsat i kernen af et befrugtet museæg. Når musen udvikler sig, bliver det fremmede DNA en del af hver celle. Disse specielt avlede mus gjorde det muligt for holdet at bruge et lægemiddel, der selektivt dræber celler, der udtrykker P16ink4a, et protein involveret i cellecyklusregulering og som nedsætter celledeling.
Efterhånden som organismer bliver ældre, øges udtrykket af P16ink4a-proteinet. Dette hjælper kroppen med at reducere proliferation af stamceller, hvilket mindsker risikoen for kræft, men samtidig gør kroppen modtagelig for virkningerne af SASP-proteinerne og andre molekyler, som disse senescente celler producerer. Fordi denne tilgang ikke kunne garantere ødelæggelsen af alle senescente celler, brugte forskerne også en kombination af lægemiddelkombinationer til at målrette de resterende senescente celler i musene. Forskerne brugte flere kohorter af ældre mus (25 til 29 måneder) samt en yngre gruppe som sammenligning.
Resultaterne var ganske klare: fjernelsen af senescente celler i kroppe og hjerner hos de ældre mus resulterede i en lindring af aldersrelateret kognitiv svækkelse, specifikt rumlig hukommelsesdysfunktion. Resultaterne viste også en reduktion i markører for senescens i neuronerne i hippocampus, en del af hjernen, der specifikt er forbundet med hukommelse og kognition, og som er udsat for progressiv forringelse med alderen.
Rydningen af de senescente celler reducerede også markant markører for hjerneinflammation, som tydeligt har været forbundet med aldersrelateret kognitiv svækkelse. Mens forfatterne understreger, at det stadig ikke er helt klart, præcis hvordan cellulær senescens påvirker hjerneældning, viser resultaterne af deres studie definitivt, at terapier rettet mod at rydde senescente celler giver en lovende tilgang til foryngelse af den aldrende hjerne samt forbedring af hukommelsen hos ældre mennesker.
NAD og cellulær senescens
Som vi har rapporteret i tidligere artikler, er NAD (nicotinamid-adenin-dinukleotid), som fungerer i kroppen som et vigtigt coenzym eller kofaktor og naturligt falder med alderen, blevet vist at have meget lovende resultater inden for anti-aging, herunder området for cellulær senescens. Forskning fra University of Queensland, Australien, offentliggjort i udgaven af Cell Reports den 18. februar 2020, viste, at relativt lave doser af NMN var effektive til at genoprette ægkvaliteten hos ældre mus. Selvom den indledende forskning blev udført på mus, er forskerne meget optimistiske med hensyn til det løfte, disse midler har i behandlingen af menneskelig fertilitet.
Forskere har afgørende vist i musemodeller, at behandling med NAD giver kraftfulde anti-aging effekter på det neurovaskulære system, herunder forbedret kognitiv ydeevne. Desuden viste behandling af vaskulære celler fra ældre rotter (den biologiske alder af 24 måneder gamle mus svarer til cirka 60-årige mennesker), som blev behandlet med NMN i fem dage, en genoprettelse af ungdommelige NAD-niveauer og tilbagevenden af mitokondriefunktion. Vi har også diskuteret andetsteds, at NAD spiller en afgørende rolle i den optimale funktion af sirtuinerne (udtales “sir-TWO-ins”), en familie af proteiner kendt som langlevethedsgenerne, som regulerer cellulær aldring.
Selvom praksisser som kalorierestriktion og faste har vist sig at øge NAD-niveauerne, er det mest pålidelige, praktiske og effektive at tage et højkvalitets NAD+ tilskud dagligt for at være sikker på, at du opfylder dine NAD-behov.
Du kan finde komplet information om alle vores kvalitets NAD+ kosttilskud her, inklusive NAD+ samt dets forløber NMN. Tages dagligt, vil NAD+ tilskud øge dine niveauer af dette kraftfulde coenzym og give dig den allerbedste beskyttelse mod aldringsprocessens virkninger, herunder aldringens skadelige virkninger på din kognitive sundhed.
Referencer:
1. Ogrodnik, M., Evans, S.A., Fielder, E., Victorelli, S., Kruger, P., Salmonowicz, H., Weigand, B.M., Patel, A.D., Pirtskhalava, T., Inman, C.L., Johnson, K.O., Dickinson, S.L., Rocha, A., Schafer, M.J., Zhu, Y., Allison, D.B., von Zglinicki, T., LeBrasseur, N.K., Tchkonia, T., Neretti, N., Passos, J.F., Kirkland, J.L. og Jurk, D. (2021), Rydning af senescente celler i hele kroppen lindrer aldersrelateret hjerneinflammation og kognitiv svækkelse hos mus. Aging Cell, 20: e13296. https://doi.org/10.1111/acel.13296.
2. Bertoldo et al. NAD-genopfyldning redder kvindelig fertilitet under reproduktiv aldring. Cell Reports, 2020; 30 (6): 1670 DOI: 10.1016/j.celrep.2020.01.058
Kiss T & Nyúl-Tóth Á et al. Nicotinamid mononukleotid (NMN) tilskud fremmer neurovaskulær foryngelse hos ældre mus: transkriptionelt fodaftryk af SIRT1 aktivering, mitokondrie beskyttelse, antiinflammatoriske og anti-apoptotiske effekter. Geroscience. 2020 Apr;42(2):527-546. doi: 10.1007/s11357-020-00165-5. Epub 2020 Feb 13. PMID: 32056076; PMCID: PMC7206476.
3. Tarantini S & Valcarcel-Ares MN et al. Nicotinamidmononukleotid (NMN) tilskud redder cerebromikrovaskulær endotel funktion og neurovaskulære koblingsreaktioner og forbedrer kognitiv funktion hos ældre mus. Redox Biol. 2019 Jun;24:101192. doi: 10.1016/j.redox.2019.101192. Epub 2019 Apr 10. PMID: 31015147; PMCID: PMC6477631.
4. Hou Y, Lautrup S, Cordonnier S, et al. NAD+ tilføjelse normaliserer Alzheimers træk. Proceedings of the National Academy of Sciences Feb 2018, 115 (8) E1876-E1885; DOI:10.1073/pnas.1718819115.
5. Kiss T, Giles C, Tarantini S. et al. Nicotinamid mononukleotid (NMN) tilskud fremmer anti-aldrings miRNA-udtryksprofil i aorta hos ældre mus, hvilket forudsiger epigenetisk foryngelse og anti-atherogene effekter. FASEB Journal 18. april 2020 https://doi.org/10.1096/fasebj.2020.34.s1.04769.


