Sejtszeneszcencia és öregedés - Mit tehet Ön
Sokan valamennyire ismerik a „szeneszcencia” szót, és az öregedéssel azonosítják a kifejezést. Végül is a szó gyökere a „sen-”, ami öreget jelent, és ugyanaz a gyökere a „szenilis” szónak is, ami természetesen az öregkor jellemzőjét jelenti.
De amikor a biológusok a sejtszeneszcenciáról beszélnek, nem pontosan az öregedésre gondolnak úgy, ahogyan az emberek általában ezt a folyamatot elképzelik. A szövet típusától függően a testben lévő sejtek különböző hosszúságú ideig élnek. A fehérvérsejtek élettartama körülbelül 13 nap, összehasonlítva a vörösvérsejtek 120 napos élettartamával. A zsírsejtek körülbelül nyolc évig élnek, míg a bélsejtek (a bélbélést kivéve) közel 16 évig élnek.
Amikor a test sejtjei elérik természetes életük végét, egy előre programozott halálon mennek keresztül egy apoptózisnak nevezett folyamat révén (ejtsd: „a-pop-TOE-sis”), amely úgy van kialakítva, hogy ne károsítson semmilyen közeli sejtet. Vagy talán egy sejt fiatal vagy középkorú, és valamilyen módon megsérül. Sokszor ez a sérülés helyrehozható, és a sejt visszatér normális működéséhez. Ha a sérülés túl súlyos, a sejt ismét apoptózison megy keresztül és elpusztul.
Normális esetben a sejtek folyamatosan osztódnak, hogy pótolják az elhalt sejteket, és segítsenek a regenerációban, például új bőrsejtek növesztésével a seb bezárásához. Néha, amikor a sejtek DNS-e megsérül, ezek a sejtek rákossá válnak, és ellenőrizetlen szaporodásba kezdenek.
A sejtszeneszcencia megértése
A másik mód, ahogyan a sejtek reagálnak a károsodásra, amely nem elég súlyos ahhoz, hogy apoptózist váltson ki, az az, hogy szeneszcenssé válnak. Ez azt jelenti, hogy ahelyett, hogy kontrollálatlan szaporodásba kezdenének, egyszerűen abbahagyják az osztódást, és a normál sejtciklus véget ér. Sok tudós úgy véli, hogy ez a képesség, hogy szeneszcens állapotba kerüljenek, a test módja annak, hogy megpróbálja megakadályozni, hogy ezek a károsodott sejtek rákossá váljanak.
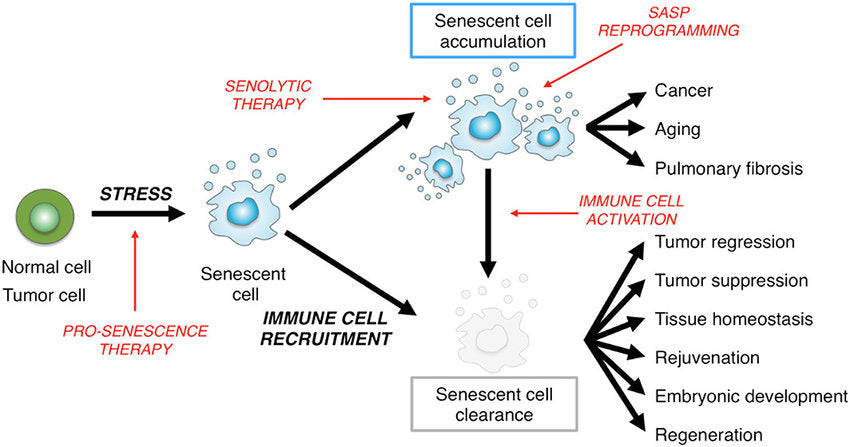
Bár ezek az öregedő sejtek nem osztódnak aktívan, semmiképpen sem halottak. Az öregedő sejtek még mindig nagyon is metabolikusan aktívak, és egy sor fehérjét és más molekulát választanak ki, amelyeket SASP-nek (senescence-associated secretory phenotype, azaz öregedéssel összefüggő szekréciós fenotípus) neveznek, ami gyulladást okozhat. Ily módon az öregedő sejtek jelezhetik az immunsejteknek, hogy jöjjenek be, segítsenek a károk eltakarításában és a szövetek helyreállításában. Eddig ez jónak tűnik.
Bár a SASP segít a szövetek helyreállításában, az ezt az együttest alkotó egyes fehérjék és molekulák káros hatásúak lehetnek. Ahogy öregszik, a szeneszcens sejtek elkezdenek felhalmozódni a testben, beleértve az agyat is. Ezek a szeneszcens sejtek mind termelik a SASP gyulladásos molekulákat és fehérjéket, amelyek valójában felgyorsíthatják magát az öregedést, és súlyosbíthatják az életkorral összefüggő állapotokat, mint például a szívbetegség és az Alzheimer-kór. Ráadásul a SASP folyamatos kitettsége valójában szeneszcenciát idézhet elő egyébként egészséges sejtekben is.
Szeneszcens sejtek eltávolítása a testből
Mi lenne, ha ezeket az öregedő sejteket el lehetne távolítani a testből, a mérgező gyulladásos SASP fehérjékkel és molekulákkal együtt, amelyeket termelnek? Már kimutatták, hogy egy neurodegeneratív betegség egérmodelljében az öregedő sejtek eltávolítása javította az állatok agyi funkcióit.
De ami nem volt ismert, az ez: vajon a szeneszcens sejtek eltávolítása a testből segíthet-e enyhíteni az agy öregedését és a normális öregedéssel járó kognitív hanyatlást? A Mayo Klinika Robert és Arlene Kogod Öregedéskutató Központjának tudósai által vezetett legújabb kutatás, amelyet az Aging Cell folyóirat 2021. január 21-i számában publikáltak, megpróbálta megválaszolni ezt a kérdést.
A kutatók ismét egy egérmodellt alkalmaztak, hogy megválaszolják ezt a kérdést. A csapat transzgenikus egereket használt. Ezeket az egereket kifejezetten orvosi kutatásokhoz tenyésztik, és „idegen” DNS-t ültetnek be egy megtermékenyített egérpetesejt magjába. Amikor az egér kifejlődik, az idegen DNS minden sejt részévé válik. Ezek a speciálisan tenyésztett egerek lehetővé tették a csapat számára, hogy egy olyan gyógyszert használjanak, amely szelektíven pusztítja el azokat a sejteket, amelyek kifejezik a P16ink4a-t, egy fehérjét, amely részt vesz a sejtciklus szabályozásában és lassítja a sejtosztódást.
Ahogy az organizmusok öregszenek, a P16ink4a fehérje kifejeződése növekszik. Ez segít a testnek csökkenteni az őssejtek szaporodását, ami csökkenti a rák kockázatát, de ugyanakkor a testet fogékonnyá teszi a SASP fehérjék és más molekulák hatásaira, amelyeket ezek az öregedő sejtek termelnek. Mivel ez a megközelítés nem tudta garantálni az összes öregedő sejt elpusztítását, a kutatók egy kombinált gyógyszerkoktélt is alkalmaztak, hogy célba vegyék a megmaradt öregedő sejteket az egerekben. A kutatók több idős egércsoportot (25-29 hónapos) használtak, valamint egy fiatalabb csoportot összehasonlításként.
Az eredmények meglehetősen egyértelműek voltak: az öregedő egerek testében és agyában lévő szeneszcens sejtek eltávolítása az életkorral összefüggő kognitív károsodás, különösen a térbeli memóriazavar enyhülését eredményezte. Az eredmények azt is kimutatták, hogy csökkentek a szeneszcencia markerei a hippocampus neuronjainál, amely az agy egy olyan része, amely kifejezetten a memóriával és a kognícióval kapcsolatos, és amely az életkor előrehaladtával fokozatosan romlik.
A szeneszcens sejtek eltávolítása szintén jelentősen csökkentette az agyi gyulladás markereit, amelyeket egyértelműen összefüggésbe hoztak az életkorral összefüggő kognitív hanyatlással. Bár a szerzők hangsúlyozzák, hogy még mindig nem teljesen világos, pontosan hogyan befolyásolja a sejtszeneszcencia az agy öregedését, tanulmányuk eredményei egyértelműen azt mutatják, hogy a szeneszcens sejtek eltávolítására irányuló terápiák ígéretes megközelítést nyújtanak az öregedő agy megfiatalítására, valamint az idősebb emberek memóriájának javítására.
NAD és a sejtszeneszcencia
Ahogy korábbi cikkekben beszámoltunk róla, a NAD (nikotinamid-adenin-dinukleotid), amely a szervezetben fontos koenzimként vagy kofaktorként működik, és természetesen csökken az életkorral, nagyon ígéretes eredményeket mutatott az öregedésgátlás területén, beleértve a sejtszeneszcencia területét is. Az Ausztráliai Queensland Egyetem kutatása, amely a Cell Reports 2020. február 18-i számában jelent meg, kimutatta, hogy a viszonylag alacsony dózisú NMN hatékony volt a petesejtek minőségének helyreállításában idős egerekben. Bár a kezdeti kutatást egereken végezték, a kutatók nagyon optimisták azzal kapcsolatban, hogy ezek az anyagok ígéretesek lehetnek az emberi termékenység kezelésében.
A kutatók meggyőzően kimutatták egérmodellekben, hogy az NAD-kezelés erőteljes öregedésgátló hatásokat fejt ki a neurovaszkuláris rendszerre, beleértve a kognitív teljesítmény javulását. Továbbá, az idős patkányok (a 24 hónapos egerek biológiai kora körülbelül a 60 éves emberekének felel meg) érrendszeri sejtjeinek öt napig tartó NMN-kezelése a fiatalos NAD-szintek helyreállítását és a mitokondriális funkció visszatérését mutatta. Máshol is tárgyaltuk, hogy az NAD kulcsszerepet játszik a szirtuinok (ejtsd: „szir-TÚ-inok”) optimális működésében, amelyek a hosszú élet génjeiként ismert fehérjecsalád, és a sejtes öregedést szabályozzák.
Bár a kalóriakorlátozás és a böjtölés növelheti az NAD szintet, a magas minőségű NAD+ kiegészítő napi szedése a legmegbízhatóbb, legpraktikusabb és leghatékonyabb módja annak, hogy biztos lehessen benne, hogy kielégíti az NAD igényeit.
Teljes körű információt találhat minden minőségi NAD+ kiegészítőnkről itt, beleértve a NAD+-t és annak előanyagát, az NMN-t. A napi szedésű NAD+ kiegészítés növeli ennek a hatékony koenzimnek a szintjét, és a lehető legjobb védelmet nyújtja az öregedési folyamat hatásai ellen, beleértve az öregedés káros hatásait a kognitív egészségre.
Hivatkozások:
1. Ogrodnik, M., Evans, S.A., Fielder, E., Victorelli, S., Kruger, P., Salmonowicz, H., Weigand, B.M., Patel, A.D., Pirtskhalava, T., Inman, C.L., Johnson, K.O., Dickinson, S.L., Rocha, A., Schafer, M.J., Zhu, Y., Allison, D.B., von Zglinicki, T., LeBrasseur, N.K., Tchkonia, T., Neretti, N., Passos, J.F., Kirkland, J.L. és Jurk, D. (2021), Az egész testre kiterjedő szeneszcens sejt eltávolítás enyhíti az életkorral összefüggő agyi gyulladást és kognitív károsodást egerekben. Aging Cell, 20: e13296. https://doi.org/10.1111/acel.13296.
2. Bertoldo et al. NAD újratöltése megmenti a női termékenységet a reproduktív öregedés során. Cell Reports, 2020; 30 (6): 1670 DOI: 10.1016/j.celrep.2020.01.058
Kiss T & Nyúl-Tóth Á et al. A nikotinamid-mononukleotid (NMN) kiegészítés elősegíti az idős egerek neurovaszkuláris megújulását: a SIRT1 aktiváció, mitokondriális védelem, gyulladáscsökkentő és anti-apoptotikus hatások transzkripciós lenyomata. Geroscience. 2020 ápr.;42(2):527-546. doi: 10.1007/s11357-020-00165-5. Epub 2020 febr. 13. PMID: 32056076; PMCID: PMC7206476.
3. Tarantini S & Valcarcel-Ares MN et al. A nikotinamid-mononukleotid (NMN) kiegészítés helyreállítja az agyi mikrokeringési endotél funkciót és a neurovaszkuláris kapcsolódási válaszokat, valamint javítja a kognitív funkciót idős egerekben. Redox Biol. 2019 Jun;24:101192. doi: 10.1016/j.redox.2019.101192. Epub 2019 Apr 10. PMID: 31015147; PMCID: PMC6477631.
4. Hou Y, Lautrup S, Cordonnier S, et al. Az NAD+ hozzáadása normalizálja az Alzheimer-jellemzőket. Proceedings of the National Academy of Sciences 2018. február, 115 (8) E1876-E1885; DOI:10.1073/pnas.1718819115.
5. Kiss T, Giles C, Tarantini S. et al. A nikotinamid-mononukleotid (NMN) kiegészítés elősegíti az öregedésgátló miRNS expressziós profilt idős egerek aortájában, előre jelezve az epigenetikai megújulást és az anti-aterogén hatásokat. FASEB Journal 2020. április 18. https://doi.org/10.1096/fasebj.2020.34.s1.04769.


